Od 9. února 2019 mají všechny složky farmaceutického dodavatelského řetězce, včetně výrobců léčiv, distributorů, velkoobchodů, lékáren a nemocnic, povinnost plnit požadavky směrnice FMD (Falsified Medicines Directive). Hlavním smyslem této směrnice je zvýšit bezpečnost výroby a dodávek léčiv v celé Evropě, chránit pacienty a bránit pronikání padělaných léčiv do dodavatelského řetězce.
Pro mnohé z těchto organizací směrnice FMD znamenala výrazné změny v jejich práci, aby dokázaly přijímat, ověřovat a vyřazovat z registru serializovaná léčiva. Zvláště pro nemocniční lékárny mohou mít zvýšené nároky na zpracování mít značný vliv na celý systém, který je pod stále větším tlakem.

Spoléhat se na ruční zpracování při zpracování serializovaných léčiv na úrovni jednotlivých balení si může vyžádat spoustu pracovních sil a času a narušovat běžný provoz. Na směrnici FMD však je možné nahlížet nejen z hlediska plnění předpisů! Organizace by měly v rámci těchto nových postupů změnit svůj přístup k celému farmaceutickému dodavatelskému řetězci.
Sébastien Sliski, General Manager Supply Chain Solutions, společnosti Zetes popisuje, jak mohou digitální inventární procesy, jako je například agregace a konsolidace, pomoci nemocničním lékárnám – a farmaceutickým velkoobchodům, které dodávají léčiva – nejen co nejlépe splnit požadavky směrnice FMD, ale navíc dosáhnout vyšší efektivity.
Nástup směrnice FMD
Směrnice FMD (Falsified Medicines Directive) je povinná pro všechny nemocniční lékárny v Evropě. Řada nemocnic, lékáren a velkoobchodů po celé Evropě však stále ještě neplní požadavky [in English]. Mnoho zemí zavedlo přechodné stabilizační období kvůli usnadnění přechodu na nová pravidla a jako prevenci proti výpadkům v zásobování léčivy. Tato období ale již brzy skončí.
Hlavním požadavkem směrnice FMD je ověřování a vyřazování léčiv z registru před vydáním pacientům – včetně péče v nemocnicích – spolu s ověřováním a dohledatelností všech léčiv na úrovni velkoobchodů.
Nemocniční lékárny musí před vydáním kontrolovat ochranné prvky ATD (Anti-Tampering Device), aby byla zaručena neporušenost balení, a změnit stav balení v národním registru NMVS (National Medicines Verification System) z „active“ na „inactive supplied“. To zahrnuje skenování 2D čárových kódů na každém balení s ověřením jedinečného identifikátoru – kterým je balení označeno od výrobce – a komunikací se systémem NMVS. Po ověření mohou být léčiva vyřazena z registru. Na rozdíl od běžné lékárny, kde mohou být léčiva vyřazena pouze v okamžiku vydání pacientovi, mohou nemocniční lékárny vyřazovat léčiva v kterékoli fázi po provedení ověření.
Vzhledem k důležitosti procesu vydávání léčiv v rámci celkové efektivity nemocnice a rostoucímu počtu složitých a speciálních produktů, které vyžadují zvláštní metody distribuce a aplikace, je naprosto klíčové tento proces správně provést hned napoprvé. Je nezbytné, aby nemocniční lékárny mohly řídit ověřování a vyřazení z registru co nejjednodušeji, protože náročné skenování léčiv na úrovni jednotlivých položek může negativně ovlivnit celý proces vydávání léčiv.
Agregace a konsolidace
Dobrou zprávou je, že to jde i bez manuálního zpracování. Technologie umožňují konsolidovat digitální informace o identifikátorech jednotlivých produktů na čárových kódech, takže nemocniční lékárna může vyřadit z registru celou dodávku jediným naskenováním.
To znamená podstatnou úsporu času a efektivity. Může to přinést výhody i pro další části dodavatelského řetězce včetně velkoobchodu, logistických partnerů a výrobce. Stačí čtyři jednoduché kroky:
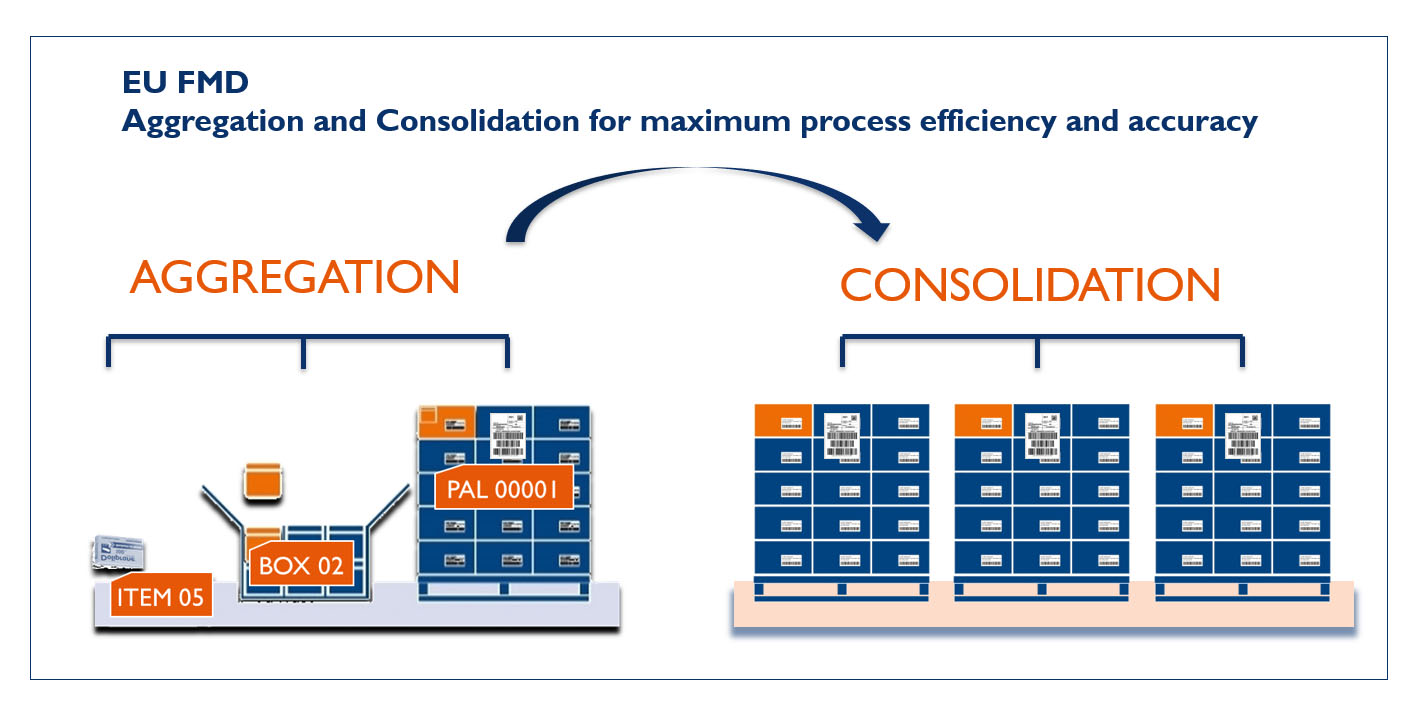
Krok 1: Agregace
Jednotlivé položky jsou naskenovány ve skladu výrobce nebo velkoobchodu a agregovány do krabic a palet. Velkoobchodu tento přístup umožňuje předem připravit dodávky a zkrátit expedici, zatímco nemocniční lékárna si může zvolit, na jaké úrovni chce provést vyřazení produktů z registru.
Krok 2: Konsolidace
Agregované položky jsou konsolidovány pod jedinečné číslo objednávky. To lze provést ve kterékoli fázi procesu skladování.
Krok 3: Komunikace
Agregované jednotky mají štítky s čárovým kódem obsahujícím jedinečné číslo objednávky. Proces expedice je také identifikován jedinečným číslem, které může být fyzicky umístěno v přepravní dokumentaci. Paralelně s tím je nemocnici zaslán digitální soubor obsahující tyto jedinečné identifikátory.
Krok 4: Náhodná kontrola a vyřazení z registru
Při příjmu dodávky má nemocnice k dispozici čárové kódy a digitální soubor, pomocí kterých může náhodně ověřit a automaticky vyřadit produkty z registru na požadované úrovni.
Využití agregace a konsolidace nejen pomáhá tím nejefektivnějším způsobem plnit požadavky směrnice FMD, ale otevírá i další možnosti k vylepšení práce lékárny a další optimalizaci procesů vydávání léčiv. Celý tento obor navíc dostal příležitost překročit hranice určované předpisy a organizačními požadavky a začít jinak nahlížet na sledovatelnost v širším farmaceutickém dodavatelském řetězci.
Závěr
Správné digitální řešení zajistí plnou viditelnost dodavatelského řetězce a zaručí, že pacienti budou mít k dispozici kvalitní a ověřená léčiva.
Základní úlohou nemocničních lékáren je včas a přesně poskytovat léčiva pacientům podle receptů. Směrnice FMD však jde ještě dál. Správné digitální řešení může pomoci zajistit plnou viditelnost dodavatelského řetězce a zaručit, že pacienti budou mít neustále k dispozici kvalitní léčiva bez rizika kontaminovaných či padělaných produktů.