Application mobile puissante et plateforme de suivi des événements
Notre approche unique totalement intégrée vous garantit une véritable tranquillité d'esprit. Elle repose sur trois piliers fondamentaux :
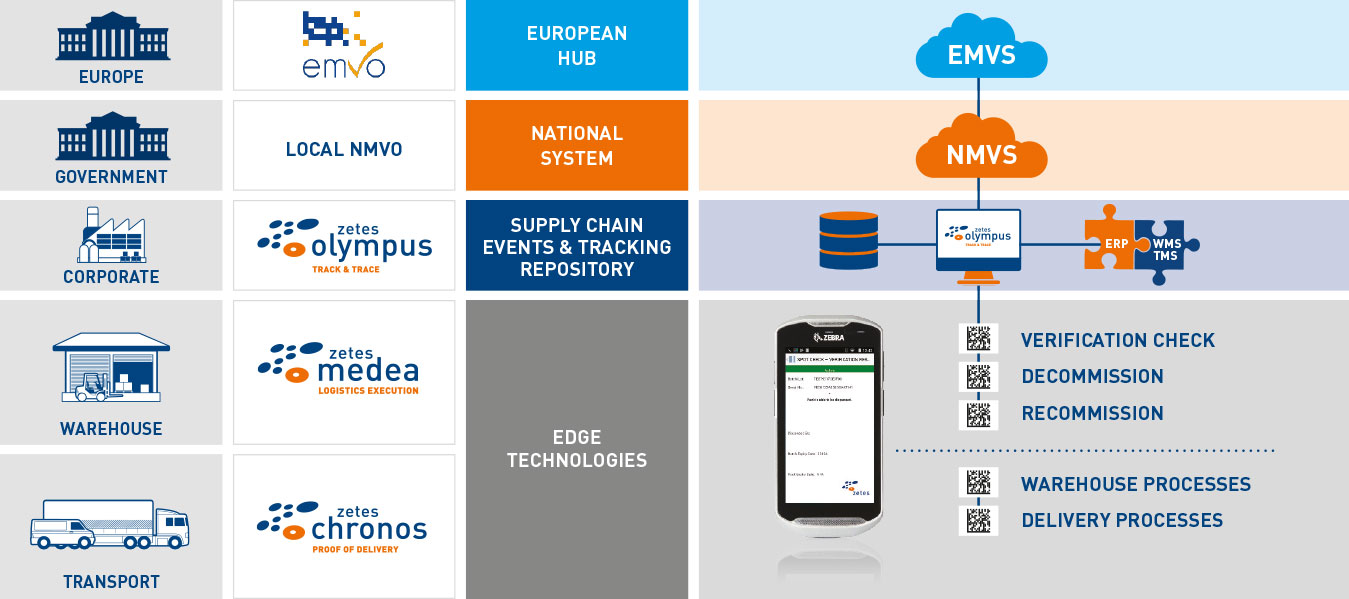
Application mobile FMD
Permet une lecture rapide et aisée des codes DataMatrix à l'aide de terminaux mobiles pour capturer les données et vérifier ou désactiver des médicaments.
1
Plateforme puissante de suivi des événements et de visibilité
Communique avec vos hubs nationaux (NMVS) et enregistre tous les événements liés à la vérification ou à la désactivation pour une période pouvant aller jusqu'à 10 ans.
2
Intégration système robuste
Notre expérience en matière d'intégration de systèmes Supply Chain, longue de plus de 30 ans, garantit une intégration transparente de notre solution avec vos systèmes existants. En adoptant notre approche éprouvée et sans risque, vous êtes certain de vous conformer aux exigences de la Directive à l'échéance prévue.
3
Tirez le meilleur parti de votre investissement
Grâce à notre approche modulaire, vous pouvez non seulement respecter le délai de mise en conformité imposé, mais aussi exploiter au mieux l'investissement consenti dans le cadre de la Directive sur les médicaments falsifiés pour une efficacité et une traçabilité optimales de l'entrepôt à la pharmacie. La solution de conformité FMD s'intègre en toute transparence avec d'autres solutions de Zetes, notamment la solution d'exécution logistique ZetesMedea pour des opérations d'entrepôt encore plus agiles et efficaces. De plus, l'intégration avec notre solution mobile de preuve de livraison ZetesChronos garantit des livraisons rapides et précises et vous offre une visibilité et une traçabilité en temps réel.
Comment pouvons-nous vous aider?
- Laboratoires et façonniers pharmaceutiques: Notre solution ZetesAtlas pour la Sérialisation pharmaceutique vous aide à rentrer en conformité avec la directive. Avec Zetes vous bénéficiez d’une approche éprouvée et d’un partenaire unique, pour réduire les risques et assurer l’implémentation sécurisée, dans les temps et à moindre coût de votre projet.
- Répartiteurs et dépositaires pharmaceutiques: Notre solution pour se conformer à la Directive sur les Médicaments Falsifiés vous permet de procéder à la vérification basée sur les risques, la désactivation, et la réactivation des étuis sérialisés au sein de l’entrepôt.
Voir la vidéoVideo